y Gestión de Procesos Farmacéuticos (en línea)
La Maestría en Buenas Prácticas de Manufactura (BPM) y Gestión de Procesos Farmacéuticos busca impactar positivamente a la industria farmacéutica, veterinaria y cosmética al formar profesionales que lideran procesos de transformación. Los egresados contribuyen a la innovación, emprendimiento y reinvención a través de la gestión operativa de procesos y el diseño de estrategias para optimizar la competitividad y el crecimiento sostenible de la industria.
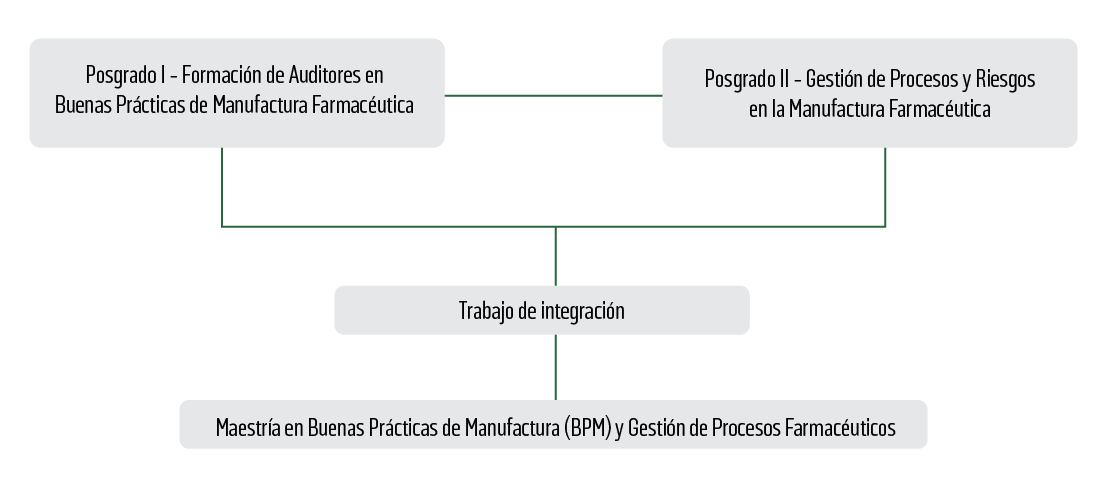
La maestría está conformada por los posgrados:
Posgrado I – Formación de Auditores en Buenas Prácticas de Manufactura Farmacéutica
Posgrado II – Gestión de Procesos y Riesgos en la Manufactura Farmacéutica
Ciencia, tecnología y salud
Áreas de formación
Gestión de riesgos
Los principios del análisis de riesgos son necesarios en la aplicación de las Buenas Prácticas de Manufactura (BPM), en los procesos de control de cambios, auditorias, desviaciones y validaciones para el aseguramiento de la calidad.
Gestión y liderazgo estratégico
Identificar posibles roles gerenciales y de liderazgo en las organizaciones para el diseño de estrategias que permitan una mejor evolución empresarial y, por ende, mayor rendimiento económico.
Gestión de procesos
La excelencia de los resultados productivos y empresariales se alcanza mediante una gestión adecuada de los procesos. Por ello, es prioritario diseñar, gestionar, evaluar y retroalimentar para la mejora continua en una organización, en cuanto a sus procesos, productos y servicios, con el objetivo de generar mayor valor para sus clientes y otros grupos de interés.
Asuntos regulatorios y de estudio de casos farmacéuticos
El quehacer profesional se relaciona con el ordenamiento jurídico de un país, ya que tanto la materia práctica como el ejercicio profesional están regulados por normas legales. En el mundo globalizado de hoy, esto cobra importancia debido a la interrelación que guardan las naciones, no solo en el intercambio de bienes, sino también de información y oportunidades de desarrollo laboral, empresarial y comercial.
Perfil de ingreso:
La Maestría en Buenas Prácticas de Manufactura (BPM) y Gestión de Procesos Farmacéuticos está dirigida a profesionales y estudiantes de Química Farmacéutica, Química, Química Biológica, Bioquímica, Veterinaria e Ingeniería Química e Industrial que se desempeñen en las áreas de:
- Procesos de auditoría e inspección de Buenas Prácticas de Manufactura
- Fabricación de productos farmacéuticos, veterinarios, cosméticos y afines
- Control y aseguramiento de calidad
- Diseño, logística y mantenimiento de plantas de producción y laboratorios de análisis, ensayo y calibración
Posgrado I – Formación de Auditores en Buenas
Prácticas de Manufactura Farmacéutica
Los profesionales egresados del Posgrado en Formación de Auditores en Buenas Prácticas de Manufactura Farmacéutica:
- Diseñan estrategias en Buenas Prácticas de Manufactura (BPM) que permitan su instauración y cumplimiento en la manufactura de medicamentos.
- Seleccionan los procesos y las condiciones que deben cumplir para la mejora continua del nivel de calidad en la fabricación de medicamentos.
- Integran las competencias desarrolladas para formar y capacitar personal en BPM para la industria farmacéutica en Guatemala, con las exigencias de los informes técnicos que se requieren en Guatemala y en el ámbito internacional
Plan de estudios
10 módulos de febrero a noviembre
- I Conceptos y Elementos Fundamentales de Buenas Prácticas de Manufactura
- II Garantía de Calidad y Alcance del Plan Maestro de Documentación
- III Conceptos de Estabilidad Farmacéutica y Mantenimiento Preventivo
- IV Autoinspección, Acciones Correctivas y Preventivas (CAPA) en los Sistemas de Gestión
- V Plan Maestro y Conceptos de Validación Farmacéutica
- VI Objetivos y Alcance de la Validación de Procesos
- VII Validación de Sistemas Críticos en la Industria Farmacéutica
- VIII Aplicación de Herramientas de Mejoramiento, Análisis de Datos y Herramientas Estadísticas en BPM
- IX Gestión Efectiva del Proceso de Auditoría y Práctica Profesional
- X Competencia del Personal e Importancia del Análisis de Riesgos en Buenas Prácticas de Manufactura y Proyecto Integrado
Posgrado II – Gestión de Procesos y Riesgos en la Manufactura Farmacéutica
Los profesionales egresados del Posgrado en Gestión de Procesos y Riesgos en la Manufactura Farmacéutica:
- Dirigen equipos multidisciplinarios que buscan el mejoramiento estratégico de empresas farmacéuticas y los diferentes servicios que se prestan al sistema de salud, relacionados con el uso racional de medicamentos.
- Diseñan programas de gestión del riesgo para su identificación, análisis, evaluación y tratamiento en los procesos y actividades que se desarrollan en la manufactura farmacéutica.
- Coordinan estrategias y procesos necesarios para el logro de objetivos para documentar y controlar los procesos productivos farmacéuticos.
Plan de estudios
7 módulos de febrero a noviembre
- I Tecnología Avanzada e Innovación Farmacéutica
- II Técnicas Analíticas para el Estudio de Casos en Manufactura Farmacéutica
- III Gestión de Procesos Farmacéuticos
- IV Gestión de Riesgos en la Manufactura Farmacéutica
- V Asuntos Regulatorios y Fundamentos de Derecho Farmacéutico en el Ámbito Internacional
- VI Gestión Estratégica y Liderazgo
- VII Proyecto integrador (tesis, ensayo o modelo de trabajo profesional)
Modalidad
Formato:
Las clases se imparten en línea.
Duración:
10 meses cada posgrado. El proyecto integrador se desarrolla desde el inicio de las actividades académicas.
Horario de clases:
Posgrado I: Cada módulo se imparte de lunes a viernes durante la primera semana del mes, de 5:00 a 9:00 p. m.
Posgrado II: Cada módulo se imparte de lunes a jueves durante tres semanas al mes, de 5:00 a 9:00 p. m.
Localización:
Plataforma virtual UVG.
Idioma:
Español.
REQUISITOS
- Completar la solicitud de admisión en el portal de admisiones en línea
- Experiencia laboral deseable
- Certificación de notas de licenciatura
- Entrevista con el coordinador del programa
- Título de pregrado con sellos de la SAT y Contraloría General de Cuentas (Títulos expedidos en el extranjero deben venir apostillados)
- Curriculum vitae
- Documento Personal de Identificación (DPI) o pasaporte (nacionalidad extranjera)
- Para cursar el posgrado II, se requiere haber aprobado el Posgrado I, debe adjuntar copia del Certificado de Auditor en BPM
Nota: Si eres egresado de otro programa académico de UVG, solo debes solicitar el cambio de carrera y realizar el pago de matrícula a través del Portal de Servicios Electrónicos.